兽医科技
2025-09-24 14:28:08

本内容于2025年9月发表在《中国兽医杂志》,文章通过从病原学检测、血清学检测和分子生物学检测方面综述了国内外ASFV检测方法的研究进展,为ASFV的科学防控提供参考,分享给感兴趣的同行阅读。
SCI猪病研究,带着偏见读文献!
摘要:非洲猪瘟(ASF)是由非洲猪瘟病毒(ASFV)引起的一种高度接触性传染病,以猪的网状内皮系统感染、高热、全身性出血等为主要临床特征,严重威胁全球养猪业可持续发展。目前尚无确实安全有效的ASF疫苗和抗病毒药物,生物安全仍是该病防控的主要和首要措施。疫病防控,检测先行,对ASFV进行及时、高效、准确的检测和监测是其生物安全防控的关键环节。本文从病原学检测、血清学检测和分子生物学检测3个方面综述了国内外ASFV检测方法的研究进展,以期为其科学防控提供参考。
关键词:非洲猪瘟(ASF);非洲猪瘟病毒(ASFV);检测方法
非洲猪瘟(African swine fever,ASF)是由非洲猪瘟病毒(African swine fever virus,ASFV)引起的猪的一种高度接触性传染病,以网状内皮系统感染、高热和全身性出血等为典型临床特征。自 1921 年肯尼亚首次报道 ASF疫情以来,该病在全球多个国家呈地方性流行,严重制约养猪业的健康发展。2018年,基因II型ASFV传入我国并在短时间内迅速扩散,重创我国生猪产业。随后,ASFV 基因II型缺失毒株、基因I型毒株在我国田间陆续出现。更为严峻的是,2021年左右出现的ASFV基因I/II型重组毒株突破了以II型毒株为基础研制的减毒疫苗的保护作用,并且已逐步取代基因II型强毒株成为主流毒株。当前,我国ASFV流行毒株呈现“多谱系、多时空”的复杂态势,使其防控面临更加严峻挑战。目前,尚无确实安全有效的ASF疫苗获批应用,生物安全体系构建仍是疫病防控的核心策略。疫病防控,检测先行,建立及时、高效、精准的ASFV检测监测体系,是生物安全防控的关键环节。
ASF与经典猪瘟、猪繁殖与呼吸综合征、猪丹毒、仔猪副伤寒、猪伪狂犬病和猪肺疫等疫病具有相似的临床症状,仅通过临床观察或尸体剖检难以进行鉴别诊断。因此,ASF的确诊不能仅依赖临床诊断,还需结合实验室诊断手段开展综合判定。目前,确诊ASF疑似病例通常需要结合至少2种实验室检测方法,例如同步检测疑似感染动物的病毒核酸和特异性抗体。在众多方法中,基于聚合酶链式反应(Polymerase chain reaction,PCR)方法检测病毒核酸被公认为是一种极为有效且实用的ASFV诊断方法。血清学检测是 ASFV流行病学调查的重要工具,可用于追溯病原侵入猪群或野猪种群的时间节点。其中,酶联免疫吸附试(Enzyme-linked immunosorbent assay,ELISA)因操作便捷,成为实际生产中检测ASFV抗体的主流方法。本文系统综述了国内外已报道的ASFV实验室检测方法,对比分析了不同方法的特点和应用局限,以期为我国ASF的综合防控策略制定提供科学参考。
1 病料采集
ASFV检测的样品采集需结合检测目的、样品病毒含量、不同监测场景和检测方法特性采取差异化的采样策略,注重规范性和质量控制,以确保检测的准确性。
1.1 样品类型选择
根据检测方法(血清学检测、核酸检测等)和病程阶段,优先选择病毒含量高、代表性强的样品。核酸检测优选样品:发病初期猪只的脾脏、扁桃体等内脏器官,病毒含量高的样品是核酸检测(如PCR等)的首选;血液、由淋巴结、肝脏等器官制备的组织液也常用于核酸检测,适用于病毒血症期的样品采集。抗体检测样品:血清、口腔液或口鼻分泌物适合采用血清学检测(如ELISA等),可反映机体免疫应答状态,但需注意感染后抗体产生存在滞后性(不适用于潜伏期检测)。现场快速检测样品:口腔拭子、直肠拭子、全血等,操作便捷,适合基层或现场快速筛查,但需注意这类样品病毒含量较低,可能导致假阴性。特殊场景样品:厨余垃圾、饲料粉尘、环境拭子等可用于追溯病毒传播途径(如饲料污染),需结合富集技术提升检测灵敏度。不同类型样品采样要求见表1。
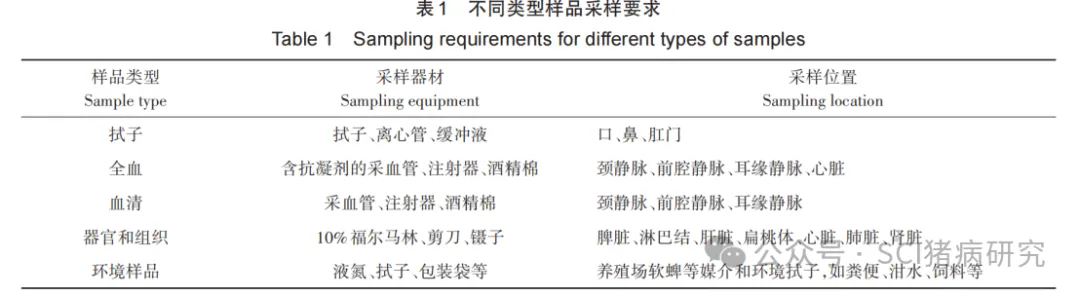
1.2 采集规范和质量控制
样品采集需使用一次性器皿(如离心管、拭子等),严禁重复使用,同时应及时更换手套以减少交叉污染,脏器样品需在无菌环境下采集以避免杂质干扰;发病初期优先采集脾脏、淋巴结等高病毒载量组织,亚急性或慢性病例可采集血液、扁桃体等样品,对疑似感染猪只建议同时采集多种样品(如脾脏和血清)以提高检出率;采样后需立即冷藏(4 ℃短期保存)或冷冻(−20 ℃及以下长期保存),全程冷链运输以避免高温导致病毒核酸或抗原降解,拭子样品需浸入专用保存液防止干燥;此外,采样时需详细记录样品信息(包括采样时间、猪只编号、样品类型、采集部位和储运条件等),建立可追溯体系以便后续结果复核和疫情追溯。综上,ASFV检测样品采集的核心是“选对样品、规范操作、严控质量”,需根据检测场景灵活选择样品类型,并通过全程质控减少干扰因素,为准确诊断提供可靠基础。
2 病原学检测方法
2.1 红细胞吸附试验(Hemadsorption test,HAD)
HAD的原理为ASFV 感染的猪巨噬细胞或单核细胞可吸附猪红细胞,从而呈现“玫瑰花环”现象。目前尚未发现其他猪源病毒具有类似特性,因此该检测方法对ASFV具有高度特异性。尽管该方法特异性强、敏感性高,但存在操作流程繁琐、检测周期较长的局限性。此外,部分 EP402R突变或缺失的ASFV基因II型和基因I型毒株,无法产生红细胞吸附现象,导致该方法对这类毒株不适用。
2.2直接免疫荧光试验(Direct immunofluorescence test,DIF)
DIF是利用荧光标记抗体检测样品中ASFV的方法。该方法具有操作简便、检测耗时短的特点,同时兼具良好的特异性和敏感性,具体应用场景包括:病理组织中ASFV抗原的定位检测、不产生红细胞吸附现象的ASFV毒株鉴定,以及细胞培养时ASFV所致细胞病变的辅助判定。然而,该方法存在以下局限性:在亚急性型和慢性型ASF病例中,DIF检测灵敏度会显著下降;此外,受限于技术原理,DIF难以实现高通量批量检测,且试验所需的高特异性ASFV荧光标记抗体存在制备难度大、获取成本高的问题。
2.3以病原为检测对象的 ELISA
ELISA 由Engvall 和Perlmann 在1971年首次提出,该方法基于抗原-抗体特异性结合原理和酶对底物的高效催化特性,可实现对样品中抗原、抗体或其他生物分子的定性检测和定量分析。1997 年,Vidal 等使用ASFV p72 蛋白的单抗建立了1种夹心ELISA 检测方法,灵敏度可达2. 3 × 102 PFU/mL。 2006年,Hutchings 等建立了 2 种检测ASFV 的间接夹心ELISA,发现采用多克隆抗体包被时的检测灵敏度显著优于单克隆抗体包被。尽管这类以抗原为检测靶标的ELISA方法适用于大规模样品筛查,但其灵敏度低于HAD 和PCR 。
3 血清学检测方法
3.1 以抗体为检测对象的ELISA
在ASF暴发早期,感染动物多表现为急性或亚急性病程,死亡率高,此时常采用分子生物学检测方法快速检出病毒,以实现疫情的早期控制。但随着疫情持续,ASFV变异毒株不断出现,越来越多的感染动物呈现隐性感染状态,甚至不表现任何临床症状。ASFV感染可诱导猪体迅速产生特异性抗体,且抗体可维持数月至数年。在未使用ASFV疫苗的前提下,抗体检测阳性即表明动物群体已被病毒感染。因此,ASFV抗体检测成为大规模流行病学筛查的关键手段,可有效补充分子生物学检测在隐性感染群体中的监测盲区。
ELISA是检测ASFV抗体的经典方法,目前主流的ASFV抗体ELISA 检测方法包括:(1)包被单一蛋白的间接ELISA。Chen等以真核表达的 ASFV p30为包被抗原,建立了1种间接ELISA检测方法,最低可检测到 1∶12 800 稀释的ASFV阳性血清。Wu等将ASFV p15与弹性蛋白样多肽(Elastin-like polypeptide)融合表达后再切除,得到了无标签的 p15,以其为包被抗原建立间接ELISA 检测方法,最低可检测到1∶1 600稀释的ASFV阳性血清。另外,还有一些检测方法将多个ASFV蛋白(如 p72、p54 和 p30)的优势抗原表位串联,设计新型抗原表位重组蛋白进行包被,基于此类重组蛋白建立间接ELISA检测方法,其最低可检测到1∶6 400稀释的ASFV阳性血清。(2)包被多种蛋白的间接ELISA。Zhou等基于ASFV p30 和 pB602L 建立了双抗原间接ELISA检测方法,最低可检测到1∶1 600 稀释的ASFV 阳性血清。Jung 等建立了1 种基于CD2v、CAP80(pB602L)、p54 和p22的间接ELISA检测方法。(3)双抗原夹心ELISA。通过原核表达并纯化ASFV p30 或者真核表达ASFV p72,将蛋白标记辣根过氧化物酶(Horseradish peroxidase,HRP),建立双抗原夹心ELISA检测方法,最低可检测到1∶1 280稀释的ASFV阳性血清。(4)阻断ELISA。Tesfagaber 等基于ASFV p72及其单抗,建立了阻断ELISA检测方法,可在ASFV 感染7~9d检出抗体。(5)竞争ELISA。研究人员筛选出针对ASFV p30和pK205R的纳米抗体,将编码该纳米抗体的基因与HRP基因连接,表达获得纳米抗体-HRP融合蛋白,以此建立竞争ELISA检测方法,最低可检测到1∶320稀释的ASFV阳性血清。
以抗体为检测对象的ELISA方法灵敏度高、成本低廉,适用于大规模筛查,但因其耗时较长、操作复杂而不适用于现场快速检测。
- 2 侧流层析试验(Lateral flow assay,LFA)
LFA是1种基于抗原-抗体特异性反应原理,借助层析技术快速检测样品中目标分析物的诊断方法,其检测结果多以试纸条形式呈现。2022年,Geng 等在检测试纸条的结合垫上添加胶体金标记的ASFV p72,检测线和质控线上分别固定金黄色葡萄球菌蛋白A和p72抗体,建立了检测ASFV抗体的方法,其灵敏度优于市售商品化试剂盒,为现场快速筛查提供了更优选择。除胶体金外,量子点、荧光微球等材料也被用于开发检测ASFV的试纸条。蛋白的选择方面,除ASFV p72外,p54、pp62、p30和融合蛋白也被应用于LFA。LFA方法优势在于操作简便、反应快速、成本较低,但灵敏度相对有限。
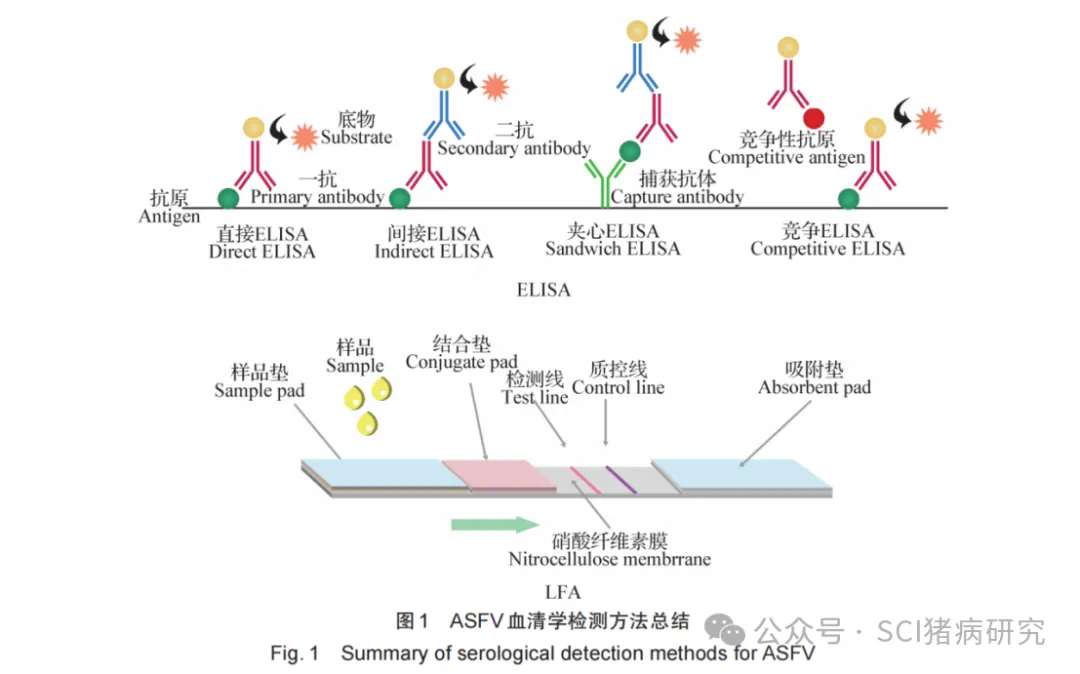
ASFV现有血清学检测方法原理总结见图1。
4 分子生物学检测方法
4.1 普通PCR和巢式PCR
PCR是通过扩增病毒特定基因片段以判断样品中是否存在目标病毒的检测方法。为提升检测效率,研究人员开发了可同时检测ASFV和猪瘟病毒(Classical swine fever virus,CSFV)的双重PCR检测方法,以及可同时检测ASFV、CSFV、猪圆环病毒2 型(Porcine circovirus type 2,PCV2)、猪繁殖与呼吸综合征病毒(Porcine reproductive and respiratory syndrome virus,PRRSV)和猪细小病毒(Porcine parvovirus,PPV)的五重PCR检测方法。
巢式PCR(Nested polymerase chain reaction)检测原理与普通PCR基本一致,其核心是反应体系中包含2对引物,其中1对引物的结合区域位于另1对引物扩增产物的内部,这种嵌套式扩增设计提升了该方法的敏感性和特异性。2006年,Basto等首次将巢式PCR用于ASFV检测,其灵敏度优于当时世界动物卫生组织(World Organization for Animal Health,WOAH)推荐的普通PCR方法。针对巢式PCR 存在加样过程中容易出现交叉污染的缺点,Milton等在2024年开发了一管式巢式PCR技术,该方法以ASFV B646L基因为检测对象,检测限可达100拷贝/反应。
普通PCR和巢式PCR的灵敏度高、特异性好,但需通过核酸电泳判定检测结果,不适用于大规模检测。
4.2 实时荧光定量PCR(Real-time fluorescent quantitativePCR,qPCR)
qPCR是在PCR 反应体系中加入荧光基团,通过实时监测荧光信号变化反映PCR产物的累积量,进而实现对起始模板定量和定性分析的技术。2010年以来,ASFV的qPCR 检测技术持续发展:2010年,McKillen 等针对B119L基因开发了基于小沟结合物的新型探针ASFV检测方法。2013年,Fernández-Pinero 等以B646L 基因为靶标,结合罗氏公司通用探针库建立了灵敏度低于18拷贝/反应的ASFV检测体系。后续研究进一步优化性能和拓展应用,2020年,Wang等开发了冻干试剂型B646L基因检测方法,该方法成本低且灵敏度优于WOAH 推荐方案。2022年,Wu等通过结合富集系统实现了水中ASFV的高效检测。2023年,Qian等建立了三重qPCR,可区分基因I 型和II 型ASFV,Hwang等则开发出仅需50min且覆盖所有24个基因型的快速ASFV检测方法。qPCR的灵敏度高于普通PCR和巢式PCR,检测结果可通过荧光信号直接呈现,被广泛应用于大规模筛查,但该方法对仪器设备要求较高,操作相对复杂。
4.3 微滴数字PCR(Droplet digitalPCR, ddPCR)
ddPCR由Hindson 等于2011年提出,该技术将核酸样品分割至众多微滴反应单元,经PCR扩增后对微滴内的荧光信号进行统计分析,从而实现核酸的绝对定量。作为第3代核酸检测技术,ddPCR能对样品中核酸进行绝对定量,在低拷贝样品检测中也表现优良。2018年,Wu等针对ASFV K205R 基因建立了ddPCR检测方法,检测下限为10拷贝/反应。此外,针对EP402R基因缺失的无血凝活性的基因II 型ASFV,Zhu等基于ASFV B646L 和EP402R基因,建立了双重ddPCR检测方法,用以区分ASFV EP402缺失型毒株与野生型毒株。
4.4 环介导等温扩增(Loop-mediated isothermal amplification, LAMP)
LAMP是Notomi 等于2000年提出的新型核酸扩增技术,其利用4种特异引物,借助链置换DNA聚合酶,在60~65℃等温条件下特异高效扩增DNA。2010年,James 等针对ASFV P1192R 基因建立了LAMP 检测方法,检测限为330拷贝/反应,结果可通过传统核酸凝胶电泳读取,还可借助qPCR仪或试纸条等读取。2020年,Wang 等针对ASFV K78R基因建立了实时LAMP 和可视化LAMP检测方法,两者检测限均为30copies/µL。2022年,Wang等针对ASFV B119L 基因建立的实时LAMP检测方法,检测限达13copies/µL。
在联用技术方面,Ji 等将LAMP与微流控结合,建立了可同时检测基因缺失型ASFV、野生型ASFV、PPV、PCV2和PRRSV 的方法;Zhu等通过将蜂巢芯片与LAMP结合,实现了对ASFV B646L、B962L、C717R、D1133L和G1340L五个基因的同步检测;Yuan等构建了基于LAMP的铋诱导增强光电化学生物传感器,通过检测光电流变化对ASFV进行定量分析;Sun等在LAMP 和LFA 方法基础上集成微加热系统,进一步提升检测效率。此外,Wang等利用LAMP 反应中会生成大量焦磷酸,导致反应体系pH值改变的特性,将LAMP与酸碱指示剂中性红结合,建立了可视化的检测方法。除传统pH指示剂外,碳纳米点(Carbon nanodots,CNDs)也可以作为酸碱指示剂。2022年,Cao 等以ASFV B646L基因为检测对象,将LAMP与CNDs结合,建立方法的检测灵敏度可达15.21copies/µL。
作为新型核酸扩增技术,LAMP 具有灵敏度高、反应速度快、反应条件温和等优势,但该方法的引物设计较为复杂。
- 5重组酶聚合酶扩增(Recombinase polymerase amplification, RPA)和重组酶介导扩增(Recombinase aided amplification, RAA)
RPA是Piepenburg等于2006年提出的等温核酸扩增技术,能在恒定温度下实现对特定核酸序列的快速扩增。针对ASFV B646L基因建立的实时RPA检测方法,检测限为3.5~100copies/µL。以ASFV CP204L基因为检测靶标建立的RPA检测方法灵敏度可达50拷贝/反应,且全过程仅需6min。RPA方法经常与LFA联合,以实现便携的可视化检测。2019年,Miao等建立的RPA-LFA检测方法以ASFV B646L基因为检测对象,检测限为150拷贝/反应。2020年,Zhai等开发的RPA-LFA 联合方法以ASFV K205R基因为检测对象,检测限为100拷贝/反应,灵敏度与qPCR相当。2021年,Wang等建立的针对ASFV B646L基因的RPA-LFA检测方法,检测限为100copies/µL。此外,Zhang等在RPA反应体系中添加SYBR Green I核酸凝胶染色剂,通过肉眼观察颜色变化即可判断检测结果。
2010年,吕蓓等对RPA进行优化,提出RAA 技术。基于此,Wu等建立针对ASFV B646L基因的实时检测方法,检测限为1 000 拷贝/反 应。2021年,Wang 等利用等温荧光扩增仪开发便携式实时RAA 方法,将检测限降至10拷贝/反应。RAA与LFA的联用技术持续发展:2021年,Zhang等建立检测ASFV B646L 基因的RAA-LFA检测方法,检测限达10 copies/µL;2022年,Wen等以ASFV B646L 基因为检测靶标,在LFA中用量子点作为显色粒子,实现了便携可视化检测,最低可识别含1拷贝ASFV基因的质粒;2023年,Zhou等在RAA体系中添加核酸外切酶III和特异性探针,不仅将检测灵敏度提升至2copies/µL,还可通过颜色变化实现可视化判读。
相较于LAMP,RPA和RAA技术具有引物设计更简便、反应条件更温和的优势,但因成本较高限制了其在大规模筛查场景中的应用。
4.6 基于CRISPR-Cas系统的核酸检测方法
规律成簇间隔短回文重复序列(Clustered regularly interspaced short palind-romic repeats, CRISPR)核酸检测技术基于CRISPR相关蛋白(CRISPR-associa-ted protein,Cas)的特异性识别和切割功能:Cas 结合靶核酸后激活非特异性切割活性,高效降解报告分子,通过信号变化实现对目标序列的高灵敏度检测。Yang等将CRISPR-Cas12a与LAMP结合,建立了ASFV检测方法,检测结果通过紫外光源照射判读,对ASFV B646L基因的最低检测限达7 copies/µL。除B646L 外,还有以KP177R、D117L等基因为检测靶标的基于CRISPR-Cas 系统的ASFV核酸检测方法。
除单基因检测外,研究人员还开发了基于CRISPR-Cas系统的多靶点检测方法。利用CRISPR-Cas12b 和CRISPR-Cas13a 分别检测ASFV MGF505-2R 和B646L基因,通过试纸条和紫外光源照射判读检测结果,且能区分野生型ASFV 和MGF505-2R缺失型ASFV。此外,Zeng等在CRISPR-Cas12a 系统中引入多个crRNA,建立针对单基因(如B646L)多位点的检测方法,该方法无需核酸扩增即可检测到低至1 pmol/L的靶标基因。
基于CRISPR-Cas系统的核酸检测结果判读方式多样:最常见的是通过紫外光源照射或试纸条;此外,还可通过肉眼观察颜色变化实现。例如,Ki等利用脲酶催化显色反应指示CRISPR-Cas12a的检测结果;Mao等将CRISPR-Cas12a与RPA结合,通过碱性磷酸酶催化显色判读结果;Zhao等利用CRISPR-Cas14a系统结合G-四联体/氯化血红素(G-quadruplex/hemin)脱氧核酶催化显色完成检测;Zhu等构建了基于CRISPR-Cas12a的金纳米颗粒(Gold nanoparticles,Au-NPs)网络比色传感平台,通过颜色变化判读结果。
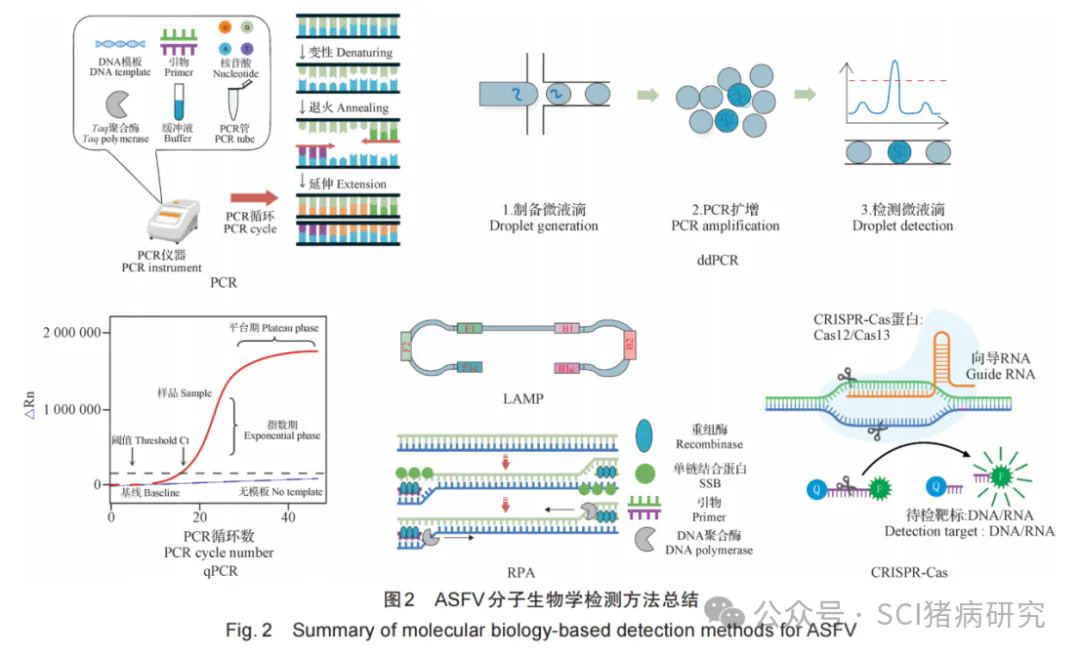
ASFV现有分子生物学检测方法原理总结见图2。
5 总结与展望
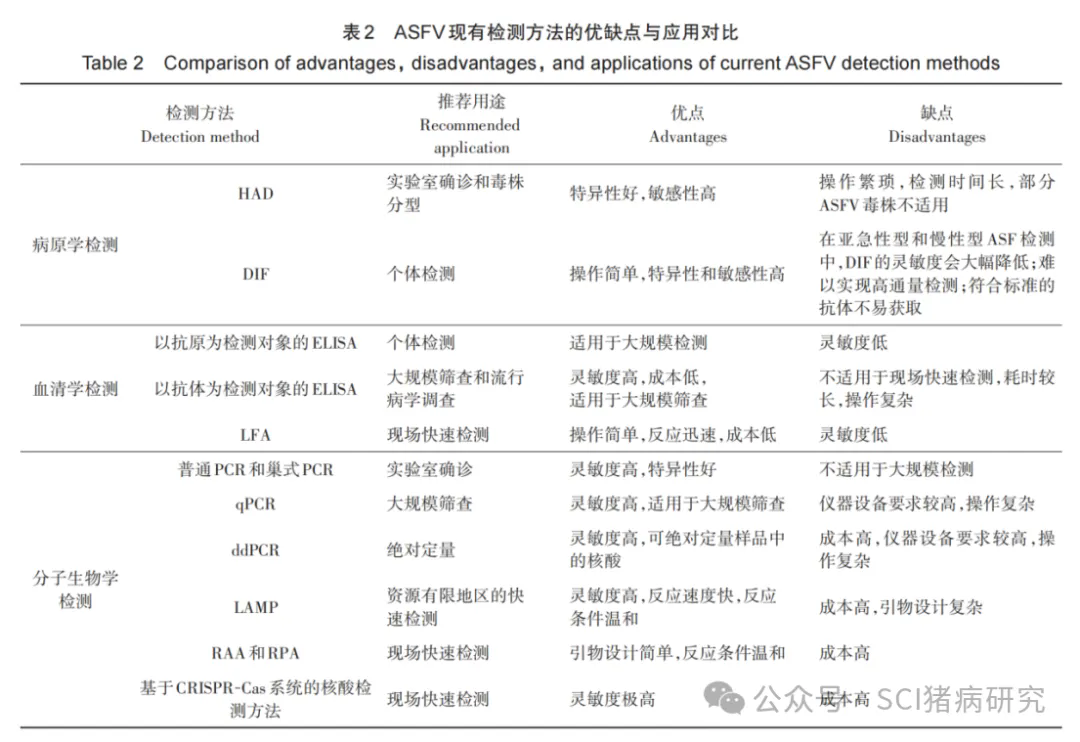
本文系统梳理了ASFV 的三大类检测技术体系,包括病原学检测、血清学检测和分子生物学检测方法,各技术的性能特点和应用局限总结见表2。
现有ASFV检测方法仍存在灵敏度不足、高通量效率有限等问题,研究人员正开发高通量、智能化等新型技术,推动检测向精准高效升级。近年来,纳米材料(石墨烯、AuNPs、量子点等)与生物传感结合,优化了检测性能,具无需标记、信号放大、微型化等优势,克服了传统方法对大型设备的依赖,为现场检测提供新方案。例如,Wang等将石墨烯场效应晶体管(Graphene field-effect transistor, G-FET)与CRISPR-Cas12a耦合,无需核酸扩增即可实现0.5 amol/L 检测限,30 min 内区分ASFV 基因I 型和II 型毒株;Zhu 等将金纳米颗粒AuNPs 与CRISPR-Cas12a 系统结合,构建可视化检测平台,实现“ 样 品 进 -结 果出 ”的 一 步 法 检 测 ,检 测 限 为0.1 copies/µL,且具备显著的现场检测适应性;Zhou等开发的基于量子点的侧向层析(Quantum dot-based lateral flow assay,QDs-LFA)试纸条,可同时检测ASFV pp62 抗体和CSFV抗体,适用于现场混合感染的快速筛查。不同检测方法的性能比较如表3所示。
值得关注的是,ASFV基因I型和II型重组毒株已逐步成为主流毒株,对现有ASFV 检测方法的稳定性和准确性构成挑战。多数分子生物学检测方法(如qPCR、RPA 和LAMP 等)靶向ASFV 保守基因(如B646L),但单一靶点的检测面对新型变异毒株存在“假阴性”风险,因此研究人员建议采用多靶点联合检测策略以提升检测的可靠性。Hu等建立的双重荧光定量PCR方法靶向ASFV MGF_110-1L 和O61R基因,可有效区分基因I型、基因II型和基因I/II 型重组毒株。血清学检测方法(如ELISA 和LFA)多以p30、p54 或pp62 等蛋白作为抗原识别位点,然而部分重组毒株可能在这些抗原区域发生抗原漂移,进而影响检测。因此,未来ASFV检测方法的靶标设计需更加关注保守性、多位点协同识别和变异区域避让,以提升检测体系对病毒变异的适应性。
为进一步提升ASFV检测方法的灵敏度、特异性和现场适用性,研究人员正在探索多元优化策略。以纳米材料界面工程为例,通过表面修饰调控可显著降低非特异性吸附干扰。Yuan等开发的光电化学生物传感器通过对材料界面的调整有效提升了检测精度。此外,将人工智能和图像识别算法嵌入试纸条判读和电信号分析,有助于规避人工判读的主观误差,提高结果一致性。低成本制造技术的推进也为新型检测平台的规模化生产提供了工艺基础。这些以材料科学、生物识别技术和微系统工程为核心的多学科交叉策略,将加速推动ASFV检测技术向高灵敏、高特异、低成本、全自动化、现场即时化的五代检测体系迭代升级。


